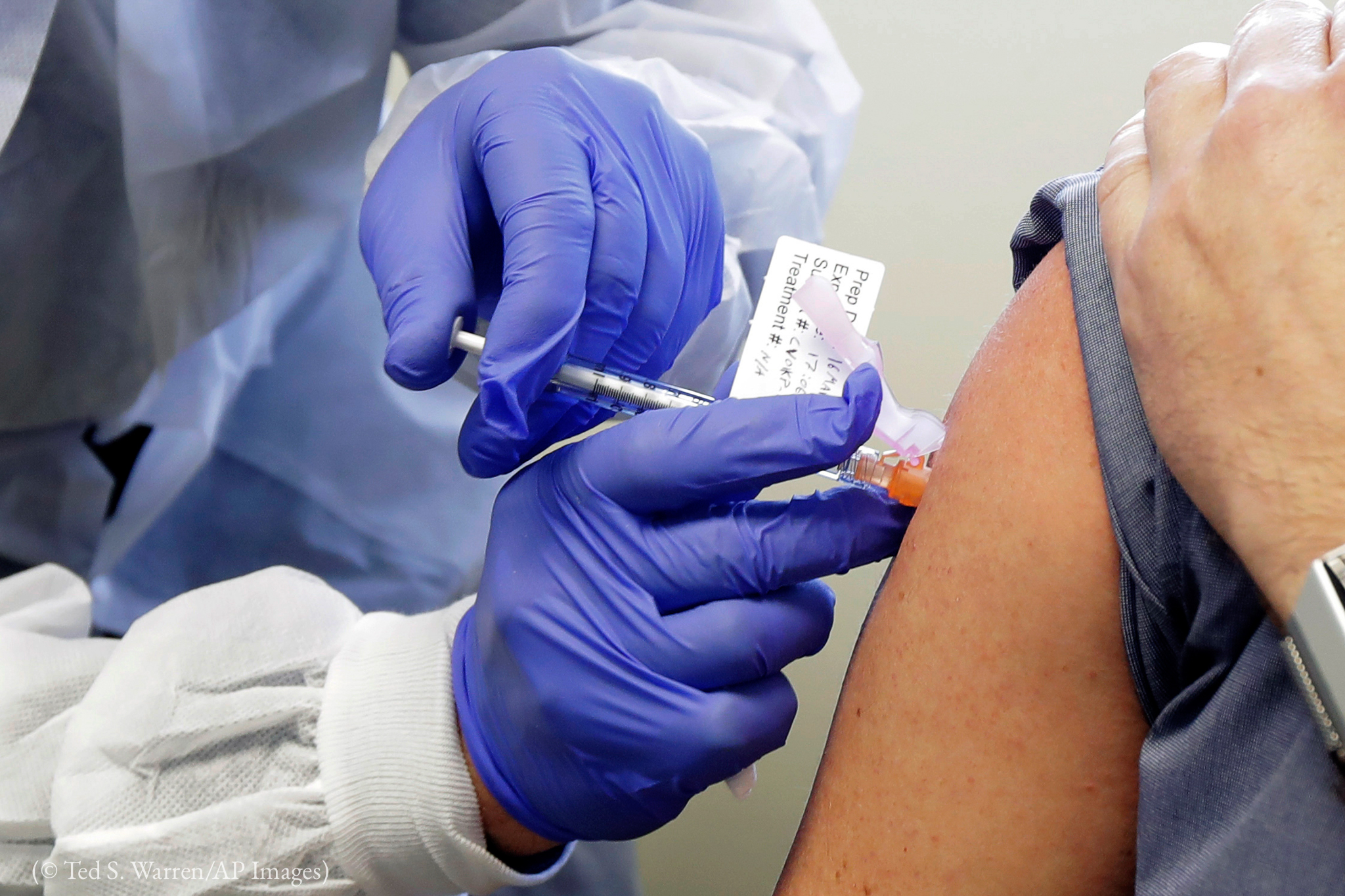
Johnson & Johnson anunció el inicio de un enorme estudio final para tratar de probar si una vacuna COVID-19 de una sola dosis puede proteger contra el virus.
El estudio será el mayor ensayo clínico de una vacuna contra el coronavirus del mundo hasta el momento, probando la fórmula en 60.000 voluntarios en los EEUU, Sudáfrica, Argentina, Brasil, Chile, Colombia, México y Perú. La cifra alrededor del doble de la cantidad de pacientes que participan en otros ensayos de fase 3.
:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/SZMXNQSWX5G7NFPB2HDRX5UEPI.jpg)
Un vial de la fórmula de Janssen, farmacéutica filial de Johnson & Johnson
La vacuna candidata consiste en vector recombinante que utiliza un adenovirus humano (el virus responsable del resfriado común) para expresar la proteína del SARS-CoV-2 en las células. El vector de adenovirus usado se ha modificado para que ya no se pueda replicar en humanos y causar enfermedad.
Los hallazgos preclínicos que ya se publicaron en la revista Nature mostraron que esta “candidata a vacuna” indujo respuestas de anticuerpos neutralizantes en macacos y proporcionó una protección completa o casi completa contra la infección por virus en los pulmones y la nariz después de la exposición al SARS-CoV-2.
El ensayo que comienza ahora está diseñado para determinar si la vacuna en investigación puede prevenir la covid-19 después de una sola dosis, a diferencia de otras candidatas que apuntan a dos aplicaciones, lo que eleva los gastos y la logística. Además, tampoco necesita ser congelada en su almacenamiento y distribución.
:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/U2TP7J25PIOUMA33DFS2TX3VII.jpg)
(Reuters)
La prueba de última etapa de J&J utilizará hasta 215 sitios en los Estados Unidos, Sudáfrica, Argentina, Brasil, Chile, Colombia, México y Perú. La compañía planea fabricar hasta mil millones de dosis en 2021, y más después de eso, dijo Paul Stoffels, director científico de J&J. Stoffels estimó que se necesitarán de seis semanas a dos meses para inscribirse en el ensayo, y dijo que la compañía espera obtener una respuesta sobre si la vacuna funciona “a finales de año o principios del próximo”.
No está claro qué tan rápido la compañía podría obtener la aprobación regulatoria, pero J&J planea fabricar dosis antes de la aprobación, por lo que podría comenzar la distribución rápidamente.
Un puñado de otras vacunas en los EEUU (desarrolladas por Moderna, Pfizer y AstraZeneca) y otras en otros países ya están en la etapa final de prueba. Hay muchas esperanzas de que las respuestas sobre al menos un candidato que se está probando en los EEUU podría llegar a finales de año, tal vez antes.
Al respecto, el epidemiólogo Anthony Fauci apuntó la probabilidad de que se requieran varios tipos de vacunas para atender la demanda mundial, y ha subrayado que la fórmula de J&J ha demostrado ya que es un fármaco “prometedor”.
Los funcionarios de salud de EEUU insisten en que la carrera por una vacuna no es una carrera de obstáculos. “Queremos hacer todo lo que podamos sin sacrificar la seguridad o la eficacia – no vamos a hacer eso – para asegurarnos de que terminemos con vacunas que van a salvar vidas”, dijo a los periodistas el médico Francis Collins, director de los Institutos Nacionales de Salud.
Pero muchos especialistas en vacunas se preguntan si la Administración de Alimentos y Medicamentos se atendrá a ese objetivo bajo la intensa presión de la administración de Trump. El presidente Donald Trump ha presentado sistemáticamente un calendario más rápido para una nueva vacuna que lo que los expertos dicen que es adecuado para probar completamente a los candidatos.
Mientras tanto, las pruebas de otra vacuna experimental, fabricada por AstraZeneca, permanecen en suspenso en los Estados Unidos mientras los funcionarios examinan una cuestión de seguridad, a pesar de que se han reanudado los estudios en otros países.
A principios de esta semana, el vicepresidente Mike Pence instó a los gobernadores de los estados a “hacer su parte para crear la confianza pública de que será una vacuna segura y eficaz”. Y Fauci añadió en el llamamiento a los gobernadores que confía en “un proceso probado y verdadero” que tiene incorporados controles y equilibrios, incluyendo una junta independiente que evalúa el progreso de cada ensayo de la vacuna, así como “la integridad de la FDA”.
Tras conocerse el ensayo de J&J, Donald Trump celebró la noticia e instó a la FDA a “actuar rápidamente”.
Incluso si la FDA permitiera el uso de emergencia de una vacuna para finales de año, los suministros serían limitados y se darían primero a los grupos vulnerables como los trabajadores de la salud. Es probable que la mayoría de los estadounidenses no reciban una vacuna hasta el año próximo.
Los Centros para el Control y la Prevención de Enfermedades quieren que los estados se preparen ahora para lanzar las vacunas, lo que presentará enormes desafíos logísticos. El miércoles, el CDC anunció la distribución de 200 millones de dólares en fondos aprobados por el Congreso para ayudar a comenzar las operaciones.
Fuente: Infobae, (con información de AP, Reuters y EFE).