En la imagen, los científicos Jia Tan, José Polo y Xiaodong (Ethan) Liu, responsables del primer modelo de embrión humano creado a partir de células de la piel. Universidad de Monash.
La creación y el desarrollo temprano de la vida humana es uno de los procesos que la ciencia tiene más dificultades para investigar. Sin embargo, las trabas para obtener embriones humanos y conocer cómo se crean o qué les afecta está ahora más cerca de terminar: un equipo de investigadores liderados por el bioquímico José Polo ha logrado crear un modelo artificial de embrión humano que puede ayudar a entender las primeras dos semanas de desarrollo de la vida.
El equipo de Polo, en la Universidad de Monash (Australia), ha conseguido crear un modelo de blastocisto – como se denomina a un embrión de seis días de vida – a partir de células de la piel humana. “Lo que hemos hecho es crear un modelo de blastocisto a partir de células de la piel humana reprogramadas a células madre pluripotentes inducidas (IPS)”, explica a El Independiente desde Australia el investigador que ha dirigido el proyecto que hoy se publica en Nature. Es la primera vez que se consigue crear un modelo de embrión humano, algo que hasta ahora sólo había conseguido en ratones el investigador español Juan Carlos Izpisúa.PUBLICIDAD
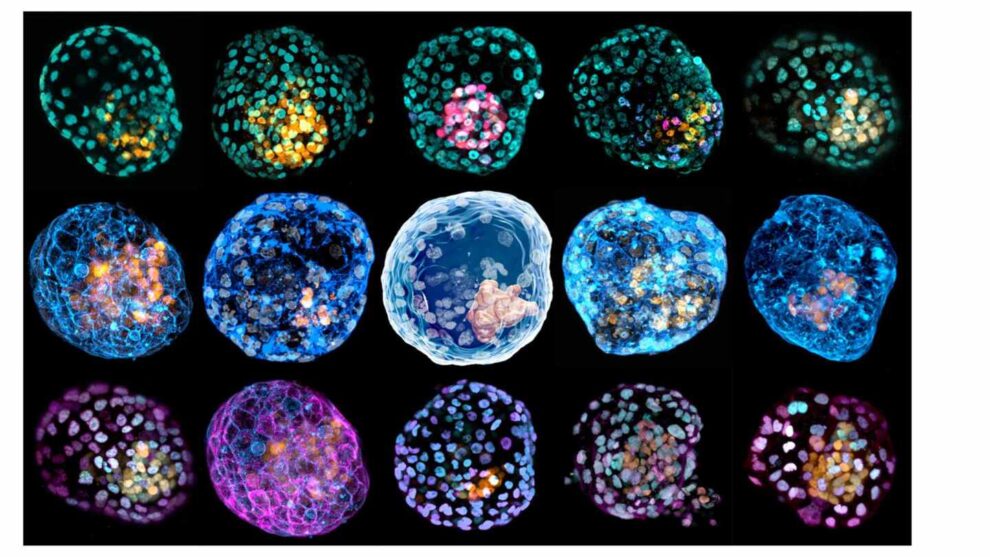
Su hallazgo empezó con un descubrimiento casi casual cuando intentaban comprender el proceso por el que las células de la piel se pueden reprogramar en células madre pluripotentes inducidas (IPS), un hallazgo por el que Yamanaka había conseguido el Nobel en 2012. «Ya el año pasado descubrimos que también podíamos hacer células de la placenta, el trofoblasto, algo que ya publicamos en Nature. Y lo que decidimos fue ver qué pasaba si en lugar de estudiar estas células que estaban siendo reprogramadas en placas de petri, que es de dos dimensiones, las poníamos una placa en forma de pirámide invertida, y que permite que las celulas interaccionen en tres dimensiones. Lo que no esperábamos era que se organizaran y formaran una estructura similar a una pelota. De hecho, cuando se formó tuvimos que hacer muchos experimentos para comprobar qué era hasta que concluimos que era un modelo de embrión», explica desde Australia a El Independiente José Polo.
Este embrión artificial no es exactamente igual que el humano en su estructura, su creación no implica a un óvulo y un espermatozoide y Polo incide en ello. «No hemos creado un embrión humano sino un modelo similar a partir de células de la piel de una persona. En la estructura por ejemplo no tiene un área llamada zona pelúcida. Le hemos denominado iblastoid en relación a las células pluripotentes IPS. Lo que hemos podido comprobar es que su desarrollo es similar al humana en los primeros 11 días y eso nos abre la puerta a poder estudiar y solucionar muchos de los problemas relacionados con los primeros días tras la concepción y el momento de la implantación», indica el investigador.
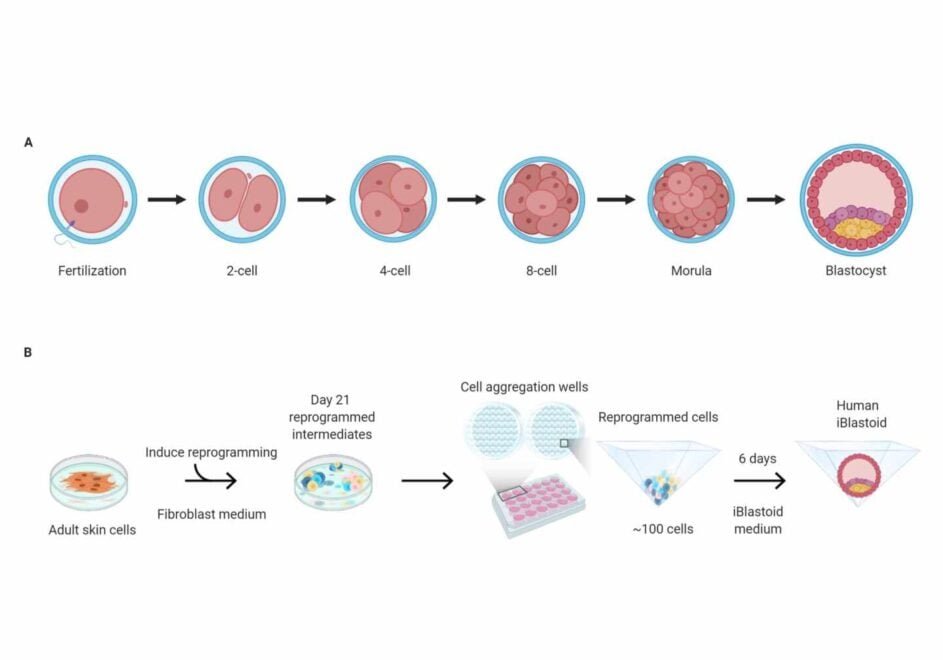
Actualmente la legislación no permite que los embriones de laboratorio se puedan desarrollar más allá de 14 días y el equipo de Polo ha eliminado los iblastoids a los 11 días. «Quiero insistir en que no es un embrión humano sino un modelo; no obstante sabemos las implicaciones éticas que tiene esto y contamos con todas las autorizaciones necesarias siendo extremadamente cuidadosos. Además, tendremos que justificar la eliminación de todos los iblastoids que creemos antes de los 14 días».
Pero, ¿se podría implantar este iblastoid en un útero y que evolucionara? Polo es tajante: «Hasta que no haces un experimento no puedes saber 100% qué ocurrirá, pero los estudios en ratones a los que se ha implantado modelos similares no han conseguido implantarse en el útero y yo estoy convencido de que no se conseguiría».
Ayudar a solucionar problemas de fertilidad
Poder crear estos modelos de embriones tempranos a gran escala plantea un gran abanico de aplicaciones que hasta ahora estaban altamente restringidas. «Para investigar en este campo sólo contábamos con embriones donados a la ciencia y lógicamente son dificilísimos de conseguir. Ahora en un platillo de café podemos tener dos o tres millones de células de la piel y conseguir cientos de iblastoids», apunta.
Estos iblastoids pueden ser clave para entender los problemas de infertilidad. «¿Sabes que entre el 25 y el 75% de las concepciones, según los estudios, se pierden en las primeras dos semanas? Las mujeres a veces ni se dan cuenta pero pueden subyacer problemas de fertilidad que con estos modelos podremos estudiar y entender con mucha más facilidad», subraya Polo.
«Quizás la mujer está tomando algún fármaco que afecta al desarrollo embrionario y no lo sabe, también podremos entender el rol de los distintos genes – tenemos más de 2o.ooo y estudiar qué mutaciones o problemas genéticos hay que se transmiten de los padres al embrión en los primeros días de desarrollo», añade el investigador.
Estos modelos de embriones también pueden ayudar a las prácticas de los profesionales que se enfrentan por primera vez al manejo de embriones, que en las clínicas de fertilidad se implantan justo a los seis días. «La presión a la que pueden enfrentarse estos profesionales, estudiar si esos blastocitos están dañados. También en universidades o laboratorios», explica Polo.
Investigar la influencia del Covid
Otro de los campos de investigación que abren los iblastoids es el de estudiar la influencia de virus o de fármacos en los primeros días de desarrollo humano. «Uno de los asuntos que vamos a investigar es si el coronavirus es capaz de afectar al blastocisto o en el momento de la implantación».
De momento, estos científicos aguardan la licencia de Australia para comenzar a producir estos iblastoids y empezar su aplicación a la ciencia: «Vamos a aprender muchísimo y ayudaremos muchísimo a todas las parejas que tienen problemas de fertilidad».
Fuente: El Independiente

